Cookie-Einstellungen
Diese Website benutzt Cookies, die für den technischen Betrieb der Website erforderlich sind und stets gesetzt werden. Andere Cookies, die den Komfort bei Benutzung dieser Website erhöhen, der Direktwerbung dienen oder die Interaktion mit anderen Websites und sozialen Netzwerken vereinfachen sollen, werden nur mit Ihrer Zustimmung gesetzt.
Konfiguration
Technisch erforderlich
Diese Cookies sind für die Grundfunktionen des Shops notwendig.
"Alle Cookies ablehnen" Cookie
"Alle Cookies annehmen" Cookie
Ausgewählter Shop
CSRF-Token
Cookie-Einstellungen
FACT-Finder Tracking
Individuelle Preise
Kundenspezifisches Caching
Session
Währungswechsel
Komfortfunktionen
Diese Cookies werden genutzt um das Einkaufserlebnis noch ansprechender zu gestalten, beispielsweise für die Wiedererkennung des Besuchers.
Facebook-Seite in der rechten Blog - Sidebar anzeigen
Merkzettel
Statistik & Tracking
Endgeräteerkennung
Kauf- und Surfverhalten mit Google Tag Manager
Partnerprogramm
| Artikelnummer | Größe | Datenblatt | Manual | SDB | Lieferzeit | Menge | Preis |
|---|---|---|---|---|---|---|---|
| I2500-01B.200 | 200 µl | - | - |
3 - 19 Werktage* |
462,00 €
|
Bei Fragen nutzen Sie gerne unser Kontaktformular.
Bestellen Sie auch per E-Mail: info@biomol.com
Größere Menge gewünscht? Bulk-Anfrage
Bestellen Sie auch per E-Mail: info@biomol.com
Größere Menge gewünscht? Bulk-Anfrage
The NF-kB/Rel transcription factors are present in the cytosol in an inactive state, complexed... mehr
Produktinformationen "IkappaB alpha Control Cell Extracts,"
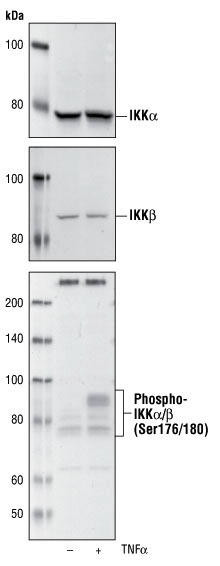
The NF-kB/Rel transcription factors are present in the cytosol in an inactive state, complexed with the inhibitory IkB proteins (1-3). Activation occurs via phosphorylation of IkB-a at Ser32 and Ser36, resulting in the release and nuclear translocation of active NF-kB (3-7). IkB-a phosphorylation and resulting Rel-dependent transcription are activated by a highly diverse group of extracellular signals, including inflammatory cytokines, growth factors and chemokines. Phosphorylation of IkB-a at Ser32 and Ser36 has been shown to stimulate conjugation with ubiquitin followed by proteasome-mediated degradation of IkB, resulting in the release of active NF-kB. Kinases that phosphorylate IkB at these activating sites have been identified (8). Because phosphorylation of IkB-a at Ser32 is essential for release of active NF-kB, phosphorylation at this site is an excellent marker of NF-kB activation (1-3). Nonphosphorylated IkB-a Control Cell Extracts: Total cell extracts from HeLa cells prepared without treatment serve as a negative control. Applications: Western Blots: As controls, we recommend using 20ul of phosphorylated and nonphosphorylated IkB-a cell extracts. Optimal dilutions to be determined by the researcher. , Storage and Stability:, May be stored at 4°C for short-term only. For long-term storage, store at -20°C. Aliquots are stable for at least 6 months at -20°C. For maximum recovery of product, centrifuge the original vial after thawing and prior to removing the cap. Further dilutions can be made in assay buffer.
| Schlagworte: | IKBA, NFKBIA, IkB-alpha, IkappaBalpha, I-kappa-B-alpha, NF-kappa-B inhibitor alpha, Major histocompatibility complex enhancer-binding protein MAD3 |
| Hersteller: | United States Biological |
| Hersteller-Nr: | I2500-01B |
Eigenschaften
| Anwendung: | WB |
Datenbank Information
| KEGG ID : | K04734 | Passende Produkte |
| UniProt ID : | P25963 | Passende Produkte |
Handhabung & Sicherheit
| Lagerung: | -20°C |
| Versand: | +4°C (International: -20°C) |
Achtung
Nur für Forschungszwecke und Laboruntersuchungen: Nicht für die Anwendung im oder am Menschen!
Nur für Forschungszwecke und Laboruntersuchungen: Nicht für die Anwendung im oder am Menschen!
Hier kriegen Sie ein Zertifikat
Loggen Sie sich ein oder registrieren Sie sich, um Analysenzertifikate anzufordern.
Bewertungen lesen, schreiben und diskutieren... mehr
Kundenbewertungen für "IkappaB alpha Control Cell Extracts,"
Bewertung schreiben
Loggen Sie sich ein oder registrieren Sie sich, um eine Produktbewertung abzugeben.
Zuletzt angesehen