Cookie-Einstellungen
Diese Website benutzt Cookies, die für den technischen Betrieb der Website erforderlich sind und stets gesetzt werden. Andere Cookies, die den Komfort bei Benutzung dieser Website erhöhen, der Direktwerbung dienen oder die Interaktion mit anderen Websites und sozialen Netzwerken vereinfachen sollen, werden nur mit Ihrer Zustimmung gesetzt.
Konfiguration
Technisch erforderlich
Diese Cookies sind für die Grundfunktionen des Shops notwendig.
"Alle Cookies ablehnen" Cookie
"Alle Cookies annehmen" Cookie
Ausgewählter Shop
CSRF-Token
Cookie-Einstellungen
FACT-Finder Tracking
Individuelle Preise
Kundenspezifisches Caching
Session
Währungswechsel
Komfortfunktionen
Diese Cookies werden genutzt um das Einkaufserlebnis noch ansprechender zu gestalten, beispielsweise für die Wiedererkennung des Besuchers.
Facebook-Seite in der rechten Blog - Sidebar anzeigen
Merkzettel
Statistik & Tracking
Endgeräteerkennung
Kauf- und Surfverhalten mit Google Tag Manager
Partnerprogramm
| Artikelnummer | Größe | Datenblatt | Manual | SDB | Lieferzeit | Menge | Preis |
|---|---|---|---|---|---|---|---|
| NSJ-R31887 | 100 µg | - | - |
3 - 10 Werktage* |
790,00 €
|
Bei Fragen nutzen Sie gerne unser Kontaktformular.
Bestellen Sie auch per E-Mail: info@biomol.com
Größere Menge gewünscht? Bulk-Anfrage
Bestellen Sie auch per E-Mail: info@biomol.com
Größere Menge gewünscht? Bulk-Anfrage
0.5mg/ml if reconstituted with 0.2ml sterile DI water. CYP1A1 is involved in phase I xenobiotic... mehr
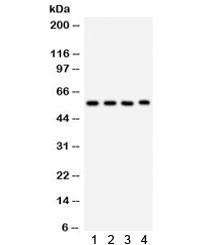
Produktinformationen "Anti-CYP1A1"
0.5mg/ml if reconstituted with 0.2ml sterile DI water. CYP1A1 is involved in phase I xenobiotic and drug metabolism (one substrate of it is theophylline). It is inhibited by fluoroquinolones and macrolides and induced by aromatic hydrocarbons. CYP1A1 is also known as AHH (aryl hydrocarbon hydroxylase). It is involved in the metabolic activation of aromatic hydrocarbons (polycyclic aromatic hydrocarbons, PAH), for example, benzo(a)pyrene (BP), by transforming it to an epoxide. In this reaction, the oxidation of benzo[a]pyrene is catalysed by CYP1A1 to form BP-7,8-epoxide, which can be further oxidized by epoxide hydrolase (EH) to form BP-7,8-dihydrodiol. Finally CYP1A1 catalyses this intermediate to form BP-7,8-dihydrodiol-9,10-epoxide, which is the ultimate carcinogen. However, an in vivo experiment with gene-deficient mice has found that the hydroxylation of benzo(a)pyrene by CYP1A1 can have an overall protective effect on the DNA, rather than contributing to potentially carcinogenic DNA modifications. This effect is likely due to the fact that CYP1A1 is highly active in the intestinal mucosa, and thus inhibits infiltration of ingested benzo(a)pyrene carcinogen into the systemic circulation. Protein function: A cytochrome P450 monooxygenase involved in the metabolism of various endogenous substrates, including fatty acids, steroid hormones and vitamins (PubMed:11555828, PubMed:14559847, PubMed:12865317, PubMed:15805301, PubMed:15041462, PubMed:18577768, PubMed:19965576, PubMed:20972997, PubMed:10681376). Mechanistically, uses molecular oxygen inserting one oxygen atom into a substrate, and reducing the second into a water molecule, with two electrons provided by NADPH via cytochrome P450 reductase (NADPH--hemoprotein reductase) (PubMed:11555828, PubMed:14559847, PubMed:12865317, PubMed:15805301, PubMed:15041462, PubMed:18577768, PubMed:19965576, PubMed:20972997, PubMed:10681376). Catalyzes the hydroxylation of carbon-hydrogen bonds. Exhibits high catalytic activity for the formation of hydroxyestrogens from estrone (E1) and 17beta-estradiol (E2), namely 2-hydroxy E1 and E2, as well as D-ring hydroxylated E1 and E2 at the C15-alpha and C16- alpha positions (PubMed:11555828, PubMed:14559847, PubMed:12865317, PubMed:15805301). Displays different regioselectivities for polyunsaturated fatty acids (PUFA) hydroxylation (PubMed:15041462, PubMed:18577768). Catalyzes the epoxidation of double bonds of certain PUFA (PubMed:15041462, PubMed:19965576, PubMed:20972997). Converts arachidonic acid toward epoxyeicosatrienoic acid (EET) regioisomers, 8,9-, 11,12-, and 14,15-EET, that function as lipid mediators in the vascular system (PubMed:20972997). Displays an absolute stereoselectivity in the epoxidation of eicosapentaenoic acid (EPA) producing the 17(R),18(S) enantiomer (PubMed:15041462). May play an important role in all-trans retinoic acid biosynthesis in extrahepatic tissues. Catalyzes two successive oxidative transformation of all-trans retinol to all-trans retinal and then to the active form all-trans retinoic acid (PubMed:10681376). May also participate in eicosanoids metabolism by converting hydroperoxide species into oxo metabolites (lipoxygenase-like reaction, NADPH-independent) (PubMed:21068195). [The UniProt Consortium]
| Schlagworte: | Anti-CYPIA1, Anti-Cytochrome P450-C, Anti-Cytochrome P450-P1, Anti-Cytochrome P450 1A1, Anti-Cytochrome P450 form 6, Anti-Hydroperoxy icosatetraenoate dehydratase, CYP1A1 Antibody |
| Hersteller: | NSJ Bioreagents |
| Hersteller-Nr: | R31887 |
Eigenschaften
| Anwendung: | WB, IHC (paraffin), (IF), FC, IF |
| Antikörper-Typ: | Polyclonal |
| Konjugat: | No |
| Wirt: | Rabbit |
| Spezies-Reaktivität: | human, mouse, rat |
| Immunogen: | Amino acids 183-320 of human CYP1A1 |
| Format: | Purified |
Datenbank Information
| KEGG ID : | K07408 | Passende Produkte |
| UniProt ID : | P04798 | Passende Produkte |
| Gene ID : | GeneID 1543 | Passende Produkte |
Handhabung & Sicherheit
| Lagerung: | +4°C |
| Versand: | +4°C (International: +4°C) |
Achtung
Nur für Forschungszwecke und Laboruntersuchungen: Nicht für die Anwendung im oder am Menschen!
Nur für Forschungszwecke und Laboruntersuchungen: Nicht für die Anwendung im oder am Menschen!
Hier folgen Informationen zur Produktreferenz.
mehr
Hier kriegen Sie ein Zertifikat
Loggen Sie sich ein oder registrieren Sie sich, um Analysenzertifikate anzufordern.
Bewertungen lesen, schreiben und diskutieren... mehr
Kundenbewertungen für "Anti-CYP1A1"
Bewertung schreiben
Loggen Sie sich ein oder registrieren Sie sich, um eine Produktbewertung abzugeben.
Zuletzt angesehen