Die Immunantwort von T-Lymphozyten wird über das Gleichgewicht zwischen Kostimulation und inhibitorischen Signalen kontrolliert. Diese Regulation wird von sogenannten Immun-Checkpoints vermittelt. Unter physiologischen Bedingungen sind Immun-Checkpoints für die Erhaltung der Immuntoleranz und dem Schutz von Gewebe während einer Infektion verantwortlich. Veränderung der inhibitorischen Immun-Checkpoints, durch monoklonale Antikörper oder lösliche Rezeptoren, zur Aktivitätssteigerung der T-Lymphozyten, bietet sich als Therapieziel bei Autoimmunerkrankungen, Tumoren, Infektionskrankheiten und Transplantationen an.
Einige Immun-Checkpoints wurden bereits für klinische Anwendungen bei Immuntherapien untersucht
- CTLA-4 (Cytotoxic T Lymphocyte Antigen-4) hat Sequenzhomologie und identische Liganden (CD80/B7-1 oder CD86/B7-2) mit dem kostimulatorischen Molekül CD28. Unterscheidet sich aber darin, seine inhibitorischen Signale an den T-Lymphozyten, auf dem es exprimiert ist, weiterzuleiten.
- PD-1 (Programmed Cell Death Protein-1) ist ein negativ kostimulatorisch wirkendes Molekül, das zwei Liganden bindet. PD-L1 (auch als B7-H1; CD274 bekannt) und PD-L2 (B7-C; CD273). Antagonistische monoklonale Antikörper gegen CTLA-4 oder PD-1 und lösliche CTLA-4 oder PD-1 Rezeptoren können mit der Fc-Region von Immunglobulinen (Ig) verbunden werden und werden zur Verbesserung der T-Lymphozyten-Toxizität gegen Tumorzellen benutzt.
- LAG-3 (Lymphocyte Activation Gene-3 Protein) ist ein CD4 ähnliches negativ regulierendes Protein mit einer hohen Affinität für MHC-II die zu Toleranz von T-Lymphozyt Proliferation und Homöostase führen. Blockierung der LAG-3/MHC-II Interaktion, mithilfe eines LAG-3-Ig Fusionsproteins, verbessert die Immunantwort gegen Tumore. Kombinatorische Blockierung des PD-1 und LAG-3 wirkt synergistisch und verringert das Wachstum von bestehenden Tumoren.
Zusätzlich kann die Blockierung anderer inhibitorischer Rezeptoren, wie BTLA (B- and T-lymphocyte attenuator), KIR (killer immunoglobulin-like receptors), TIM-3 (T-cell immunoglobulin and mucin domain-containing protein 3), A2aR (adenosine 2A receptor) und B7-H3 oder H4 (Mitglieder der B7-Familie), die Immunität gegen Tumore erhöhen. Dies kann mit einzelnen, aber auch durch Kombination mit einem zweiten Immun-Checkpoint-Inhibitor passieren. Bei kostimulatorischen Signalproteinen, zu denen ICOS (inducible T cell costimulator), CD28 oder Mitglieder der TNF-Superfamilie (4-1BB (CD137), OX40, CD27 oder CD40) zählen, konnte gezeigt werden, dass diese für allergische und autoimmune Reaktionen, sowie Entzündungen mitverantwortlich sind.

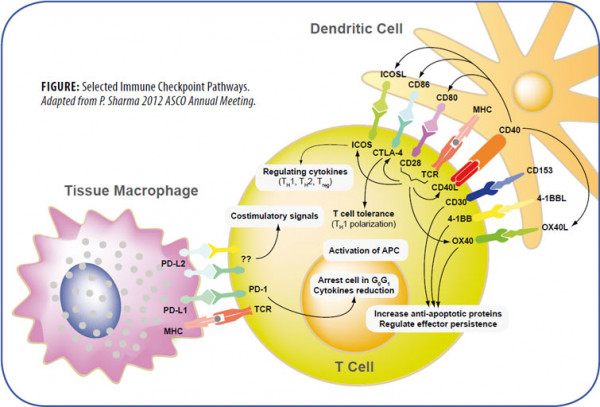
Abbildung. Regulation und Aktivierung von T-Lymphozyten hängt von T-Zell-Rezeptor (TCR) Signalen und kostimulatorischen Rezeptoren, die negative (-) oder positive (+) Signale senden, ab.
Die B7-CD28 Superfamilie
Die B7 Familie besteht aus strukturverwandten Zell-Oberflächen Liganden, die an immun-regulatorische Lymphozyt-Rezeptoren binden. Aktivierung von T- und B-Lymphozyten beginnt mit der Bindung der T- oder B-Zell-Rezeptoren, die letztendliche Immunantwort wird aber von zusätzlichen Signalen der B7-Liganden bestimmt. Diese kostimulatorischen oder koinhibitorischen Signale der B7-Liganden werden durch die Rezeptoren der CD28-Familie der Lymphozyten vermittelt, zusätzlich lösen die Signale auch Interleukin Produktion aus. Die Interaktion zwischen B7-Liganden mit kostimulatorischen Rezeptoren verstärkt die Immunantwort, die Interaktion mit koinhibitorischen Rezeptoren schwächt sie ab. Zur Zeit gibt es sieben Mitglieder der B7-Familie: B7.1 (CD80), B7.2 (CD86), inducible costimulator ligand (ICOS-L), programmed death-1 Ligand (PD-L1), programmed death-2 Ligand (PD-L2), B7-H3 und B7-H4. Zusätzlich gibt es vier CD28-Rezeptoren: CD28, CTLA-4 (CD152), ICOS und PD-1. Wie wichtig die B7-CD28-Superfamilie für die Regulation der Immunantwort ist, zeigt sich an der Entwicklung von Immundefizienz und Autoimmunerkrankung bei Veränderung der Signale, die von B7 Liganden ausgehen. Damit ist die B7-Familie ein wichtiges Ziel für Thehrapieansätze.
Kostimulatorische Rezeptoren der TIM Familie
Die TIM (T cell/transmembrane, immunoglobulin and mucin) Familie spielt eine wichtige Rolle bei der Regulation der Immunantwort. Allergie-Reaktionen, Asthma, Immuntoleranz bei Transplantationen, Autoimmunerkrankung und die Antwort auf virale Infektionen werden alle durch durch die TIM mitreguliert. Die einzigartige Struktur der TIM immunglobulin variablen Region Domäne ermöglicht die hochspezifische Erkennung von Posphatidylserin (PtdSer) auf der Oberfläche von apoptotischen Zellen. TIM-1, kritisch bei Asthma und Allergie, wird vor allem von TH2-Helfer Zellen exprimiert und fungiert als Kostimulator bei der Aktivierug von T-Lymphozyten. TIM-3 wird von TH1- und TC1-Zellen exprimiert und ist für das inhibitorische Signal verantwortlich, das zur Apoptose dieser zellen führt. TIM-3 wird außerdem von einigen dendritischen Zellen exprimiert und vermittelt die Phagozytose von apoptotischen Zellen und Antigenpräsentation auf MHC-I. TIM-4 wird einzig auf Antigen präsentierenden Zellen exprmiert und vermittelt die Phagozytose von apoptotischen Zellen, sowie der Aufrechterhaltung der Eigentoleranz.

![CD152 [CTLA-4] -muIg Fusion Protein, (human), Biotin conjugated CD152 [CTLA-4] -muIg Fusion Protein, (human), Biotin conjugated](https://www.biomol.com/media/image/ae/57/3b/ANC-501-030_200x200.png)



![Anti-CD272 [BTLA] (human), clone ANC6E9, Biotin conjugated Anti-CD272 [BTLA] (human), clone ANC6E9, Biotin conjugated](https://www.biomol.com/media/image/06/19/db/ANC-272-030_200x200.png)
![Anti-CD134 [OX40] (human), clone BerAct35, Biotin conjugated Anti-CD134 [OX40] (human), clone BerAct35, Biotin conjugated](https://www.biomol.com/media/image/9f/9c/9c/ANC-355-030_200x200.png)

![CD28:B7-1[Biotinylated] Inhibitor Screening Assay Kit CD28:B7-1[Biotinylated] Inhibitor Screening Assay Kit](https://www.biomol.com/media/image/93/e7/9f/BPS-72007_200x200.jpg)